Formula oxidului de sulf, proprietăți, riscuri și utilizări
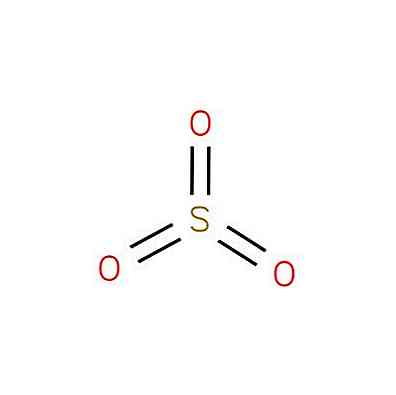
oxid de sulf (VI), cunoscut și ca trioxid de sulf sau anhidridă sulfurică, este un compus chimic cu formula SO3. Structura sa este prezentată în Figura 1 (EMBL-EBI, 2016).
Trioxidul de sulf este produs într-o formă gazoasă diluată, într-o instalație de acid sulfuric de contact prin oxidarea gazelor care conțin dioxid de sulf.
Până în prezent, însă, singurul preparat de trioxid de sulf pur din gazele care conțin SO3 diluat, a fost un proces la scară pilot care implică condensarea crioscopică.
Procedura obișnuită implică în schimb distilarea oleiului. Căldura necesară pentru distilarea oleiului este cea mai convenabil furnizată de gazul de contact fierbinte din instalația de acid sulfuric asociată.
Acesta poate fi preparat în laborator prin încălzirea acidului sulfuric fumător și colectarea sublimatului într-un receptor răcit. Dacă vaporii se condensează peste 27 ° C, forma gama se obține ca lichid.
Dacă aburul se condensează sub 27 ° C și în prezența unei urme de umiditate, se obține un amestec al celor trei forme. Cele 3 forme pot fi separate prin distilare fracționată.
Proprietățile fizice și chimice ale oxidului de sulf
Trioxidul de sulf are formă de ace albe care se transformă în fum în aer. Se întâlnește de multe ori inhibitori pentru prevenirea polimerizării (Centrul Național pentru Biotehnologia Informației, 2017).
Greutatea sa moleculară este 80.066 g / mol, densitatea este de 1,92 g / cm³ g / ml și de topire puncte și puncte de fierbere sunt 16,8 ° C și respectiv 44,7 ° C. (Societatea Regală de Chimie, 2015).
Compusul este combinat cu apă cu forță explozivă, formând acid sulfuric datorită acidității sale. Trioxidul de sulf carbonizează substanțele organice.
Trioxidul de sulf absoarbe umezeala rapid, emițând fumuri albe dense. Soluțiile de trioxid de sulf în acid sulfuric se numesc acid sulfuric fumigant sau oleum. (Trioxid de sulf, 2016).
Reacția trioxidului de sulf și difluorură de oxigen este foarte viguros si explozii au loc în cazul în care reacția este efectuată în absența unui solvent. Reacția excesului de trioxid de sulf cu tetrafluoretilenă determină descompunerea explozivă a fluorurii de carbonil și a dioxidului de sulf.
Reacția acidului percloric anhidru cu trioxidul de sulf este violentă și este însoțită de evoluția căldurii considerabile. Lichidul de trioxid de sulf reacționează violent cu clorura de nitril, chiar la 75 ° C.
Reacția de trioxid de sulf și oxid de plumb provoacă luminiscență albă. Combinația dintre iod, piridină, trioxid de sulf și formamidă a generat un gaz peste presiune după câteva luni.
Acest lucru se datorează formării lentă de acid sulfuric, apă sau formamidă deshidratant extern la acidul cianhidric (Trioxid, S.F.).
Reactivitate și pericole
trioxid de sulf este un compus stabil incompatibil cu materiale organice, fin metale sub formă de pulberi, baze, apa, cianurile și o largă varietate de alte substanțe chimice.
Substanța este un oxidant puternic și reacționează violent cu materiale combustibile și reducătoare și cu compuși organici care provoacă incendii și explozii.
Reacționează violent cu apă și cu aer umed pentru a produce acid sulfuric. Soluția în apă este un acid puternic, reacționează violent cu baze și sunt metale corozive care formează gaz inflamabil / exploziv.
Compusul este corosiv pentru metale și țesături. Cauzează arsuri la ochi și la piele. Ingerarea provoacă arsuri grave în gură, esofag și stomac. Vaporii sunt foarte toxici prin inhalare. (Institutul Național pentru Siguranța și Sănătatea Ocupațională, 2015)
În cazul contactului cu ochii, trebuie să verificați dacă purtați lentile de contact și să le eliminați imediat. Ochii trebuie spălați cu apă curentă timp de cel puțin 15 minute, ținând pleoapele deschise. Puteți folosi apă rece. Unguentul nu trebuie utilizat pentru ochi.
Dacă produsul chimic vine în contact cu hainele, scoateți-l cât mai repede posibil, protejându-vă mâinile și corpul. Așezați victima sub un duș de siguranță.
Dacă produsul se acumulează pe pielea expusă a victimei, cum ar fi mâinile, spălați ușor și cu atenție pielea contaminată cu apă curgătoare și săpun neabraziv. Puteți folosi apă rece. Dacă iritația persistă, solicitați asistență medicală. Spălați hainele contaminate înainte de reutilizare.
În cazul inhalării, victima ar trebui să aibă dreptul de a se odihni într-o zonă bine ventilată. În cazul în care inhalarea este severă, victima trebuie evacuată într-o zonă sigură cât mai curând posibil. Slăbiți îmbrăcămintea strânsă cum ar fi gulerul cămășii, centurile sau cravată
Dacă victima găsește dificil să respire, oxigenul trebuie administrat. Dacă victima nu respiră, se face o resuscitare de la gură la gură.întotdeauna luând în considerare faptul că poate fi periculos pentru persoana care acordă un ajutor pentru a da resuscitare gura la gura atunci când materialul inhalat este toxic, infecțioase sau corozive.
În toate cazurile, ar trebui să se solicite asistență medicală imediată (Fișa tehnică de securitate a produsului Trioxid de sulf, 2013).
aplicații
Trioxidul de sulf este un reactiv esențial în reacțiile de sulfonare. Aceste procese oferă detergenți, coloranți și produse farmaceutice. Acesta este generat in situ din acid sulfuric sau utilizat ca soluție de acid sulfuric fuming.
Poluarea aerului cu oxizi de sulf reprezintă o problemă majoră de mediu, cu milioane de tone de dioxid de sulf și trioxid de carbon emise în atmosferă în fiecare an. Acești compuși sunt nocivi pentru viața plantelor și animalelor, precum și pentru multe materiale de construcție.
O altă mare problemă de luat în considerare este ploaia acidă. Ambii oxizi de sulf se dizolvă în picături de apă atmosferică pentru a forma soluții acide care pot fi foarte dăunătoare atunci când sunt distribuite sub formă de ploaie.
Se crede că acidul sulfuric este cauza principală a acidității ploii acide, care poate deteriora pădurile și poate provoca moartea peștilor în multe lacuri.
Acidul este, de asemenea, coroziv pentru metale, calcar și alte materiale. Posibilele soluții la această problemă sunt scumpe datorită dificultății de a elimina sulful din cărbune și de ulei înainte de ardere (Zumdahl, 2014).
referințe
- EMBL-EBI. (2016, 2 decembrie). trioxid de sulf. Adus de la ChEBI: ebi.ac.uk
- Fis¸a˘ Tehnica˘ de Securitate În conformitate cu Directiva EC 91/155 / EEC (2013, 21 mai). Adus de la sciencelab: sciencelab.com
- Centrul National de Informare Biotehnologica. (2017, 24 iunie). Baze de date compuse PubChem; CID = 24682 . Adus de la PubChem: pubchem.ncbi.nlm.nih.gov
- Institutul Național de Siguranță și Sănătate Ocupațională. (2015, 22 iulie). TRIOXID DE SULFURĂ. Adus de la cdc.gov: cdc.gov
- Societatea Regală de Chimie. (2015). Trioxid de sulf. Recuperat de la chemspider: chemspider.com
- Trioxid de sulf. (2016). Adus de la chimicale: chembook.com.
- TRIOXID DE SULFURĂ. (S.F.). Adus de la CAMEO: cameochemicals.noaa.gov.
- Zumdahl, S. S. (2014, 13 februarie). Adus de la britannica: britannica.com.


